早教吧作业答案频道 -->化学-->
为了测定某碳酸钠样品中碳酸钠的质量分数(假设杂质不溶于水,也不与其他物质反应),某化学小组进行了如下实验:请回答下列问题:(1)写出上述反应的化学方程式;(2)根据氯
题目详情
为了测定某碳酸钠样品中碳酸钠的质量分数(假设杂质不溶于水,也不与其他物质反应),某化学小组进行了如下实验:
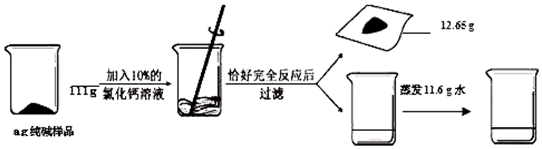
请回答下列问题:
(1)写出上述反应的化学方程式___;
(2)根据氯化钙的质量列出求解样品中纯碱的质量(x)比例式;___
(3)样品中碳酸钠的质量分数为___;
(4)若将反应后的滤液恒温蒸发掉11.6g水,则最终所得不饱和溶液中溶质的质量分数为___;
(5)若用上述纯碱样品132.5t制取烧碱,则可制得纯度为80%的烧碱___t.为了测定某碳酸钠样品中碳酸钠的质量分数(假设杂质不溶于水,也不与其他物质反应),某化学小组进行了如下实验:

请回答下列问题:
(1)写出上述反应的化学方程式___;
(2)根据氯化钙的质量列出求解样品中纯碱的质量(x)比例式;___
(3)样品中碳酸钠的质量分数为___;
(4)若将反应后的滤液恒温蒸发掉11.6g水,则最终所得不饱和溶液中溶质的质量分数为___;
(5)若用上述纯碱样品132.5t制取烧碱,则可制得纯度为80%的烧碱___t.


请回答下列问题:
(1)写出上述反应的化学方程式___;
(2)根据氯化钙的质量列出求解样品中纯碱的质量(x)比例式;___
(3)样品中碳酸钠的质量分数为___;
(4)若将反应后的滤液恒温蒸发掉11.6g水,则最终所得不饱和溶液中溶质的质量分数为___;
(5)若用上述纯碱样品132.5t制取烧碱,则可制得纯度为80%的烧碱___t.为了测定某碳酸钠样品中碳酸钠的质量分数(假设杂质不溶于水,也不与其他物质反应),某化学小组进行了如下实验:

请回答下列问题:
(1)写出上述反应的化学方程式___;
(2)根据氯化钙的质量列出求解样品中纯碱的质量(x)比例式;___
(3)样品中碳酸钠的质量分数为___;
(4)若将反应后的滤液恒温蒸发掉11.6g水,则最终所得不饱和溶液中溶质的质量分数为___;
(5)若用上述纯碱样品132.5t制取烧碱,则可制得纯度为80%的烧碱___t.

▼优质解答
答案和解析
碳酸钠和氯化钙反应生成氯化钠和碳酸钙沉淀,对应的化学方程式为Na22CO33+CaCl22═CaCO33↓+2NaCl;
设碳酸钠的质量为x,生成的氯化钠的质量为y,碳酸钙的质量为z
氯化钙的质量为111g×10%=11.1g
Na22CO33+CaCl22═CaCO33↓+2NaCl
106 111 100 117
x 11.1g z y
=
=
=
x=10.6g
y=11.7g
z=10g
样品中碳酸钠的质量分数为
×100%=80%;
(4)若将反应后的滤液恒温蒸发掉11.6g水,则最终所得不饱和溶液中溶质的质量分数为
×100%=11.7%;
(5)若用上述纯碱样品132.5t制取烧碱,设可制得纯度为80%的烧碱 的质量为a.
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
106 80
132.5t×80% 80% a
=
a=100t
故答案:
(1)Na2CO3+CaCl2═CaCO3↓+2NaCl;
(2)
=
(3)80%;
(4)11.7%;
(5)100t.
106 x 106 106 106x x x=
=
=
x=10.6g
y=11.7g
z=10g
样品中碳酸钠的质量分数为
×100%=80%;
(4)若将反应后的滤液恒温蒸发掉11.6g水,则最终所得不饱和溶液中溶质的质量分数为
×100%=11.7%;
(5)若用上述纯碱样品132.5t制取烧碱,设可制得纯度为80%的烧碱 的质量为a.
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
106 80
132.5t×80% 80% a
=
a=100t
故答案:
(1)Na2CO3+CaCl2═CaCO3↓+2NaCl;
(2)
=
(3)80%;
(4)11.7%;
(5)100t.
111 11.1g 111 111 11111.1g 11.1g 11.1g=
=
x=10.6g
y=11.7g
z=10g
样品中碳酸钠的质量分数为
×100%=80%;
(4)若将反应后的滤液恒温蒸发掉11.6g水,则最终所得不饱和溶液中溶质的质量分数为
×100%=11.7%;
(5)若用上述纯碱样品132.5t制取烧碱,设可制得纯度为80%的烧碱 的质量为a.
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
106 80
132.5t×80% 80% a
=
a=100t
故答案:
(1)Na2CO3+CaCl2═CaCO3↓+2NaCl;
(2)
=
(3)80%;
(4)11.7%;
(5)100t.
100 z 100 100 100z z z=
x=10.6g
y=11.7g
z=10g
样品中碳酸钠的质量分数为
×100%=80%;
(4)若将反应后的滤液恒温蒸发掉11.6g水,则最终所得不饱和溶液中溶质的质量分数为
×100%=11.7%;
(5)若用上述纯碱样品132.5t制取烧碱,设可制得纯度为80%的烧碱 的质量为a.
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
106 80
132.5t×80% 80% a
=
a=100t
故答案:
(1)Na2CO3+CaCl2═CaCO3↓+2NaCl;
(2)
=
(3)80%;
(4)11.7%;
(5)100t.
117 y 117 117 117y y y
x=10.6g
y=11.7g
z=10g
样品中碳酸钠的质量分数为
×100%=80%;
(4)若将反应后的滤液恒温蒸发掉11.6g水,则最终所得不饱和溶液中溶质的质量分数为
×100%=11.7%;
(5)若用上述纯碱样品132.5t制取烧碱,设可制得纯度为80%的烧碱 的质量为a.
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
106 80
132.5t×80% 80% a
=
a=100t
故答案:
(1)Na2CO3+CaCl2═CaCO3↓+2NaCl;
(2)
=
(3)80%;
(4)11.7%;
(5)100t.
10.6g 10.6g+12.65g-10g 10.6g 10.6g 10.6g10.6g+12.65g-10g 10.6g+12.65g-10g 10.6g+12.65g-10g×100%=80%;
(4)若将反应后的滤液恒温蒸发掉11.6g水,则最终所得不饱和溶液中溶质的质量分数为
×100%=11.7%;
(5)若用上述纯碱样品132.5t制取烧碱,设可制得纯度为80%的烧碱 的质量为a.
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
106 80
132.5t×80% 80% a
=
a=100t
故答案:
(1)Na2CO3+CaCl2═CaCO3↓+2NaCl;
(2)
=
(3)80%;
(4)11.7%;
(5)100t.
11.7g 10.6g+111g-10g-11.6g 11.7g 11.7g 11.7g10.6g+111g-10g-11.6g 10.6g+111g-10g-11.6g 10.6g+111g-10g-11.6g×100%=11.7%;
(5)若用上述纯碱样品132.5t制取烧碱,设可制得纯度为80%的烧碱 的质量为a.
Na22CO33+Ca(OH)22=CaCO33↓+2NaOH
106 80
132.5t×80% 80% a
=
a=100t
故答案:
(1)Na2CO3+CaCl2═CaCO3↓+2NaCl;
(2)
=
(3)80%;
(4)11.7%;
(5)100t.
106 80 106 106 10680 80 80=
a=100t
故答案:
(1)Na2CO3+CaCl2═CaCO3↓+2NaCl;
(2)
=
(3)80%;
(4)11.7%;
(5)100t.
132.5t×80% 80%a 132.5t×80% 132.5t×80% 132.5t×80%80%a 80%a 80%a
a=100t
故答案:
(1)Na22CO33+CaCl22═CaCO33↓+2NaCl;
(2)
=
(3)80%;
(4)11.7%;
(5)100t.
106 111 106 106 106111 111 111=
(3)80%;
(4)11.7%;
(5)100t.
x 11.1g x x x11.1g 11.1g 11.1g
(3)80%;
(4)11.7%;
(5)100t.
碳酸钠和氯化钙反应生成氯化钠和碳酸钙沉淀,对应的化学方程式为Na22CO33+CaCl22═CaCO33↓+2NaCl;
设碳酸钠的质量为x,生成的氯化钠的质量为y,碳酸钙的质量为z
氯化钙的质量为111g×10%=11.1g
Na22CO33+CaCl22═CaCO33↓+2NaCl
106 111 100 117
x 11.1g z y
| 106 |
| x |
| 111 |
| 11.1g |
| 100 |
| z |
| 117 |
| y |
x=10.6g
y=11.7g
z=10g
样品中碳酸钠的质量分数为
| 10.6g |
| 10.6g+12.65g-10g |
(4)若将反应后的滤液恒温蒸发掉11.6g水,则最终所得不饱和溶液中溶质的质量分数为
| 11.7g |
| 10.6g+111g-10g-11.6g |
(5)若用上述纯碱样品132.5t制取烧碱,设可制得纯度为80%的烧碱 的质量为a.
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
106 80
132.5t×80% 80% a
| 106 |
| 80 |
| 132.5t×80% |
| 80%a |
a=100t
故答案:
(1)Na2CO3+CaCl2═CaCO3↓+2NaCl;
(2)
| 106 |
| 111 |
| x |
| 11.1g |
(3)80%;
(4)11.7%;
(5)100t.
| 106 |
| x |
| 111 |
| 11.1g |
| 100 |
| z |
| 117 |
| y |
x=10.6g
y=11.7g
z=10g
样品中碳酸钠的质量分数为
| 10.6g |
| 10.6g+12.65g-10g |
(4)若将反应后的滤液恒温蒸发掉11.6g水,则最终所得不饱和溶液中溶质的质量分数为
| 11.7g |
| 10.6g+111g-10g-11.6g |
(5)若用上述纯碱样品132.5t制取烧碱,设可制得纯度为80%的烧碱 的质量为a.
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
106 80
132.5t×80% 80% a
| 106 |
| 80 |
| 132.5t×80% |
| 80%a |
a=100t
故答案:
(1)Na2CO3+CaCl2═CaCO3↓+2NaCl;
(2)
| 106 |
| 111 |
| x |
| 11.1g |
(3)80%;
(4)11.7%;
(5)100t.
| 111 |
| 11.1g |
| 100 |
| z |
| 117 |
| y |
x=10.6g
y=11.7g
z=10g
样品中碳酸钠的质量分数为
| 10.6g |
| 10.6g+12.65g-10g |
(4)若将反应后的滤液恒温蒸发掉11.6g水,则最终所得不饱和溶液中溶质的质量分数为
| 11.7g |
| 10.6g+111g-10g-11.6g |
(5)若用上述纯碱样品132.5t制取烧碱,设可制得纯度为80%的烧碱 的质量为a.
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
106 80
132.5t×80% 80% a
| 106 |
| 80 |
| 132.5t×80% |
| 80%a |
a=100t
故答案:
(1)Na2CO3+CaCl2═CaCO3↓+2NaCl;
(2)
| 106 |
| 111 |
| x |
| 11.1g |
(3)80%;
(4)11.7%;
(5)100t.
| 100 |
| z |
| 117 |
| y |
x=10.6g
y=11.7g
z=10g
样品中碳酸钠的质量分数为
| 10.6g |
| 10.6g+12.65g-10g |
(4)若将反应后的滤液恒温蒸发掉11.6g水,则最终所得不饱和溶液中溶质的质量分数为
| 11.7g |
| 10.6g+111g-10g-11.6g |
(5)若用上述纯碱样品132.5t制取烧碱,设可制得纯度为80%的烧碱 的质量为a.
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
106 80
132.5t×80% 80% a
| 106 |
| 80 |
| 132.5t×80% |
| 80%a |
a=100t
故答案:
(1)Na2CO3+CaCl2═CaCO3↓+2NaCl;
(2)
| 106 |
| 111 |
| x |
| 11.1g |
(3)80%;
(4)11.7%;
(5)100t.
| 117 |
| y |
x=10.6g
y=11.7g
z=10g
样品中碳酸钠的质量分数为
| 10.6g |
| 10.6g+12.65g-10g |
(4)若将反应后的滤液恒温蒸发掉11.6g水,则最终所得不饱和溶液中溶质的质量分数为
| 11.7g |
| 10.6g+111g-10g-11.6g |
(5)若用上述纯碱样品132.5t制取烧碱,设可制得纯度为80%的烧碱 的质量为a.
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
106 80
132.5t×80% 80% a
| 106 |
| 80 |
| 132.5t×80% |
| 80%a |
a=100t
故答案:
(1)Na2CO3+CaCl2═CaCO3↓+2NaCl;
(2)
| 106 |
| 111 |
| x |
| 11.1g |
(3)80%;
(4)11.7%;
(5)100t.
| 10.6g |
| 10.6g+12.65g-10g |
(4)若将反应后的滤液恒温蒸发掉11.6g水,则最终所得不饱和溶液中溶质的质量分数为
| 11.7g |
| 10.6g+111g-10g-11.6g |
(5)若用上述纯碱样品132.5t制取烧碱,设可制得纯度为80%的烧碱 的质量为a.
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
106 80
132.5t×80% 80% a
| 106 |
| 80 |
| 132.5t×80% |
| 80%a |
a=100t
故答案:
(1)Na2CO3+CaCl2═CaCO3↓+2NaCl;
(2)
| 106 |
| 111 |
| x |
| 11.1g |
(3)80%;
(4)11.7%;
(5)100t.
| 11.7g |
| 10.6g+111g-10g-11.6g |
(5)若用上述纯碱样品132.5t制取烧碱,设可制得纯度为80%的烧碱 的质量为a.
Na22CO33+Ca(OH)22=CaCO33↓+2NaOH
106 80
132.5t×80% 80% a
| 106 |
| 80 |
| 132.5t×80% |
| 80%a |
a=100t
故答案:
(1)Na2CO3+CaCl2═CaCO3↓+2NaCl;
(2)
| 106 |
| 111 |
| x |
| 11.1g |
(3)80%;
(4)11.7%;
(5)100t.
| 106 |
| 80 |
| 132.5t×80% |
| 80%a |
a=100t
故答案:
(1)Na2CO3+CaCl2═CaCO3↓+2NaCl;
(2)
| 106 |
| 111 |
| x |
| 11.1g |
(3)80%;
(4)11.7%;
(5)100t.
| 132.5t×80% |
| 80%a |
a=100t
故答案:
(1)Na22CO33+CaCl22═CaCO33↓+2NaCl;
(2)
| 106 |
| 111 |
| x |
| 11.1g |
(3)80%;
(4)11.7%;
(5)100t.
| 106 |
| 111 |
| x |
| 11.1g |
(3)80%;
(4)11.7%;
(5)100t.
| x |
| 11.1g |
(3)80%;
(4)11.7%;
(5)100t.
看了 为了测定某碳酸钠样品中碳酸钠...的网友还看了以下:
一题初三化学题会的来看下测P654在下列盐的水溶液中,若滴入氢氧化钠溶液产生蓝色沉淀,若滴入硝酸银 2020-05-21 …
一题关于化学溶解平衡的题.25℃时1升溶液中各含0.001摩尔氯离子和碘离子溶液中逐滴加入硝酸银( 2020-05-22 …
高碘酸钠、高锰酸钠和高氯酸钠溶液分别是什么颜色啊?高氯酸钠溶液不是黄色的吗?关于氯的化合物的溶液有 2020-06-21 …
(2012•鞍山一模)铝制品却不宜长时间盛放腌制食品.资料显示:“铝制品表面虽然有一层致密的氧化膜 2020-06-22 …
氯气是一种黄绿色的气体,水溶液叫做氯水.把品红试纸(用品红溶液浸泡而制得的试纸)伸入氯水中,品红褪 2020-07-05 …
A三甲基一氯硅属于有机物B三甲基一氯硅由碳,氢,硅,氯四种原子构成C三甲基一氯硅溶于水,所得溶液P 2020-07-06 …
关于沉淀溶解平衡和滴定比如溶液中有氯离子和碘离子,我往里加硝酸银,那这个时候肯定是碘化银先沉淀,这个 2020-11-01 …
关于溶解度的问题氯化钠在水温O℃时的溶解度是35.7左右,当温度降低到零度以下,水冻结成冰时,会有氯 2020-12-07 …
阅读下列文字,回答问题:二氧化氯(化学符号:ClO2)是一种黄绿色、有刺激性气味的气体,熔点-59. 2021-01-10 …
铝制品却不宜长时间盛放腌制食品.资料显示:“铝制品表面虽然有一层致密的氧化膜保护……氯化钠也会破坏氧 2021-01-13 …