早教吧作业答案频道 -->化学-->
实验室用50mL0.50mol•L-1盐酸、50mL0.55mol•L-1NaOH溶液和如图所示装置,进行测定中和热的实验,得到表中的数据:实验次数起始温度t1/℃终止温度t2/℃盐酸NaOH溶液120.
题目详情
实验室用50mL 0.50 mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和如图所示装置,进行测定中和热的实验,得到表中的数据:
完成下列问题:
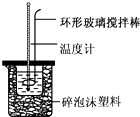
(1)不能用铜丝搅拌棒代替环形玻璃搅拌棒的理由是___.
(2)在操作正确的前提下,提高中和热测定准确性的关键是___.大烧杯如不盖硬纸板,求得的中和热数值将___(填“偏大”、“偏小”或“无影响”).结合日常生活实际该实验在___中(家用产品)效果更好.
(3)根据上表中所测数据进行计算,则该实验测得的中和热△H=___[盐酸和NaOH溶液的密度按1g•cm-3计算,反应后混合溶液的比热容(c)按4.18J•(g•℃)-1计算].
(4)如用0.5mol/L的盐酸与NaOH固体进行实验,则实验中测得的“中和热”数值将____(填“偏大”、“偏小”、“不变”).如改用60mL0.5mol/L的盐酸与50mL 0.55mol•L-1 的NaOH 溶液进行反应,与上述实验相比,所放出的热量___(填“相等”或“不相等”),所求中和热___(填“相等”或“不相等”).
(5)若某同学利用上述装置做实验,有些操作不规范,造成测得中和热的数值偏低,请你分析可能的原因是___.
A.测量盐酸的温度后,温度计没有用水冲洗干净
B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
C.做本实验的当天室温较高
D.将50mL0.55mol/L氢氧化钠溶液取成了50mL0.55mol/L的氨水
E.在量取盐酸时仰视计数
F.大烧杯的盖板中间小孔太大.-1-1
实验次数 起始温度t1/℃ 终止温度t2/℃ 盐酸 NaOH溶液 1 20.2 20.3 23.7 2 2 20.3 20.5 23.8 3 21.5 21.6 24.9 实验次数 起始温度t1/℃ 终止温度t2/℃ 实验次数 起始温度t1/℃ 1终止温度t2/℃ 2 盐酸 NaOH溶液 盐酸 NaOH溶液 1 20.2 20.3 23.7 1 20.2 20.3 23.7 2 2 20.3 20.5 23.8 2 2 20.3 20.5 23.8 3 21.5 21.6 24.9 3 21.5 21.6 24.9

-3-1
-1
| 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | NaOH溶液 | ||
| 1 | 20.2 | 20.3 | 23.7 |
| 2 2 | 20.3 | 20.5 | 23.8 |
| 3 | 21.5 | 21.6 | 24.9 |

(1)不能用铜丝搅拌棒代替环形玻璃搅拌棒的理由是___.
(2)在操作正确的前提下,提高中和热测定准确性的关键是___.大烧杯如不盖硬纸板,求得的中和热数值将___(填“偏大”、“偏小”或“无影响”).结合日常生活实际该实验在___中(家用产品)效果更好.
(3)根据上表中所测数据进行计算,则该实验测得的中和热△H=___[盐酸和NaOH溶液的密度按1g•cm-3计算,反应后混合溶液的比热容(c)按4.18J•(g•℃)-1计算].
(4)如用0.5mol/L的盐酸与NaOH固体进行实验,则实验中测得的“中和热”数值将____(填“偏大”、“偏小”、“不变”).如改用60mL0.5mol/L的盐酸与50mL 0.55mol•L-1 的NaOH 溶液进行反应,与上述实验相比,所放出的热量___(填“相等”或“不相等”),所求中和热___(填“相等”或“不相等”).
(5)若某同学利用上述装置做实验,有些操作不规范,造成测得中和热的数值偏低,请你分析可能的原因是___.
A.测量盐酸的温度后,温度计没有用水冲洗干净
B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
C.做本实验的当天室温较高
D.将50mL0.55mol/L氢氧化钠溶液取成了50mL0.55mol/L的氨水
E.在量取盐酸时仰视计数
F.大烧杯的盖板中间小孔太大.-1-1
| 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | NaOH溶液 | ||
| 1 | 20.2 | 20.3 | 23.7 |
| 2 2 | 20.3 | 20.5 | 23.8 |
| 3 | 21.5 | 21.6 | 24.9 |

-3-1
-1
▼优质解答
答案和解析
(1)不能将环形玻璃搅拌棒改为铜丝搅拌棒,因为铜丝搅拌棒是热的良导体;
故答案为:Cu传热快,热量损失大;
(2)在中和反应中,必须确保热量不散失,应提高装置的保温效果;大烧杯上如不盖硬纸板,会使一部分热量散失,求得的中和热数值将会减小;在日常生活实际该实验在保温杯中效果更好;
故答案为:提高装置的保温效果;偏小;保温杯;
(3)第1次实验盐酸和NaOH溶液起始平均温度为20.25℃,反应前后温度差为:3.45℃;
第2次实验盐酸和NaOH溶液起始平均温度为20.40℃,反应前后温度差为:3.40℃;
第3次实验盐酸和NaOH溶液起始平均温度为21.55℃,反应前后温度差为:3.35℃;
三次温度差的平均值为3.40℃,
50mL 0.50 mol•L-1-1盐酸、50mL 0.55mol•L-1-1 NaOH溶液的质量m=100mL×1g/mL=100g,c=4.18J/(g•℃),代入公式Q=cm△T得生成0.025mol的水放出热量Q=4.18J/(g•℃)×100g×3.40℃=1421.2J=1.4212KJ,即生成0.025mol的水放出热量1.4212KJ,所以生成1mol的水放出热量为
=56.8kJ,即该实验测得的中和热△H=-56.8kJ/mol;
故答案为:-56.8kJ/mol;
(4)氢氧化钠固体溶于水,放出热量,所以实验中测得的“中和热”数值将偏大;反应放出的热量和所用酸以及碱的量的多少有关,改用60mL0.5mol/L的盐酸与50mL 0.55mol•L-1 的NaOH 溶液进行反应,与上述实验相比,生成水的量增多,所放出的热量偏高,但中和热是指稀强酸与稀强碱发生中和反应生成1molH2O放出的热量,与酸碱的用量无关,测得中和热数值相等,
故答案为:偏大,不相等,相等;
(5)A.测量盐酸的温度后,温度计没有用水冲洗干净,在测碱的温度时,会发生酸和碱的中和,温度计示数变化值减小,导致实验测得中和热的数值偏小,故A正确;
B、把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓,会导致一部分能量的散失,导致实验测得中和热的数值偏小,故B正确;
C、做本实验的室温和反应热的数据之间无关,故C错误;
D、将50mL0.55mol/L氢氧化钠溶液取成了50mL0.55mol/L的氨水,由于氨水是弱碱,弱碱电离要吸热,导致实验测得中和热的数值偏小,故D正确;
E、在量取盐酸时仰视计数,会使得实际量取体积高于所要量的体积,算过量,可以保证碱全反应,导致实验测得中和热的数值偏高,故E错误;
F、大烧杯的盖板中间小孔太大,会导致一部分能量散失,导致实验测得中和热的数值偏小,故F正确;
故选:ABDF.
1.4212kJ×1mol 0.025mol 1.4212kJ×1mol 1.4212kJ×1mol 1.4212kJ×1mol0.025mol 0.025mol 0.025mol=56.8kJ,即该实验测得的中和热△H=-56.8kJ/mol;
故答案为:-56.8kJ/mol;
(4)氢氧化钠固体溶于水,放出热量,所以实验中测得的“中和热”数值将偏大;反应放出的热量和所用酸以及碱的量的多少有关,改用60mL0.5mol/L的盐酸与50mL 0.55mol•L-1-1 的NaOH 溶液进行反应,与上述实验相比,生成水的量增多,所放出的热量偏高,但中和热是指稀强酸与稀强碱发生中和反应生成1molH22O放出的热量,与酸碱的用量无关,测得中和热数值相等,
故答案为:偏大,不相等,相等;
(5)A.测量盐酸的温度后,温度计没有用水冲洗干净,在测碱的温度时,会发生酸和碱的中和,温度计示数变化值减小,导致实验测得中和热的数值偏小,故A正确;
B、把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓,会导致一部分能量的散失,导致实验测得中和热的数值偏小,故B正确;
C、做本实验的室温和反应热的数据之间无关,故C错误;
D、将50mL0.55mol/L氢氧化钠溶液取成了50mL0.55mol/L的氨水,由于氨水是弱碱,弱碱电离要吸热,导致实验测得中和热的数值偏小,故D正确;
E、在量取盐酸时仰视计数,会使得实际量取体积高于所要量的体积,算过量,可以保证碱全反应,导致实验测得中和热的数值偏高,故E错误;
F、大烧杯的盖板中间小孔太大,会导致一部分能量散失,导致实验测得中和热的数值偏小,故F正确;
故选:ABDF.
故答案为:Cu传热快,热量损失大;
(2)在中和反应中,必须确保热量不散失,应提高装置的保温效果;大烧杯上如不盖硬纸板,会使一部分热量散失,求得的中和热数值将会减小;在日常生活实际该实验在保温杯中效果更好;
故答案为:提高装置的保温效果;偏小;保温杯;
(3)第1次实验盐酸和NaOH溶液起始平均温度为20.25℃,反应前后温度差为:3.45℃;
第2次实验盐酸和NaOH溶液起始平均温度为20.40℃,反应前后温度差为:3.40℃;
第3次实验盐酸和NaOH溶液起始平均温度为21.55℃,反应前后温度差为:3.35℃;
三次温度差的平均值为3.40℃,
50mL 0.50 mol•L-1-1盐酸、50mL 0.55mol•L-1-1 NaOH溶液的质量m=100mL×1g/mL=100g,c=4.18J/(g•℃),代入公式Q=cm△T得生成0.025mol的水放出热量Q=4.18J/(g•℃)×100g×3.40℃=1421.2J=1.4212KJ,即生成0.025mol的水放出热量1.4212KJ,所以生成1mol的水放出热量为
| 1.4212kJ×1mol |
| 0.025mol |
故答案为:-56.8kJ/mol;
(4)氢氧化钠固体溶于水,放出热量,所以实验中测得的“中和热”数值将偏大;反应放出的热量和所用酸以及碱的量的多少有关,改用60mL0.5mol/L的盐酸与50mL 0.55mol•L-1 的NaOH 溶液进行反应,与上述实验相比,生成水的量增多,所放出的热量偏高,但中和热是指稀强酸与稀强碱发生中和反应生成1molH2O放出的热量,与酸碱的用量无关,测得中和热数值相等,
故答案为:偏大,不相等,相等;
(5)A.测量盐酸的温度后,温度计没有用水冲洗干净,在测碱的温度时,会发生酸和碱的中和,温度计示数变化值减小,导致实验测得中和热的数值偏小,故A正确;
B、把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓,会导致一部分能量的散失,导致实验测得中和热的数值偏小,故B正确;
C、做本实验的室温和反应热的数据之间无关,故C错误;
D、将50mL0.55mol/L氢氧化钠溶液取成了50mL0.55mol/L的氨水,由于氨水是弱碱,弱碱电离要吸热,导致实验测得中和热的数值偏小,故D正确;
E、在量取盐酸时仰视计数,会使得实际量取体积高于所要量的体积,算过量,可以保证碱全反应,导致实验测得中和热的数值偏高,故E错误;
F、大烧杯的盖板中间小孔太大,会导致一部分能量散失,导致实验测得中和热的数值偏小,故F正确;
故选:ABDF.
| 1.4212kJ×1mol |
| 0.025mol |
故答案为:-56.8kJ/mol;
(4)氢氧化钠固体溶于水,放出热量,所以实验中测得的“中和热”数值将偏大;反应放出的热量和所用酸以及碱的量的多少有关,改用60mL0.5mol/L的盐酸与50mL 0.55mol•L-1-1 的NaOH 溶液进行反应,与上述实验相比,生成水的量增多,所放出的热量偏高,但中和热是指稀强酸与稀强碱发生中和反应生成1molH22O放出的热量,与酸碱的用量无关,测得中和热数值相等,
故答案为:偏大,不相等,相等;
(5)A.测量盐酸的温度后,温度计没有用水冲洗干净,在测碱的温度时,会发生酸和碱的中和,温度计示数变化值减小,导致实验测得中和热的数值偏小,故A正确;
B、把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓,会导致一部分能量的散失,导致实验测得中和热的数值偏小,故B正确;
C、做本实验的室温和反应热的数据之间无关,故C错误;
D、将50mL0.55mol/L氢氧化钠溶液取成了50mL0.55mol/L的氨水,由于氨水是弱碱,弱碱电离要吸热,导致实验测得中和热的数值偏小,故D正确;
E、在量取盐酸时仰视计数,会使得实际量取体积高于所要量的体积,算过量,可以保证碱全反应,导致实验测得中和热的数值偏高,故E错误;
F、大烧杯的盖板中间小孔太大,会导致一部分能量散失,导致实验测得中和热的数值偏小,故F正确;
故选:ABDF.
看了 实验室用50mL0.50mo...的网友还看了以下:
下列说法中,正确的是()A.相同质量的同一溶质的饱和溶液一定比它的不饱和溶液所含的溶质多B.在一定 2020-04-09 …
250C,将O.4mol/LCH3COOH溶液和O.2mol/LNaOH溶液各1OOmL混合后,p 2020-05-13 …
11.2克铁数与200克稀硫酸恰好完全反应求产生氢气的质量?所用硫酸溶液中溶质质量分数?所得溶液溶 2020-05-14 …
1、将100g98%的浓硫酸稀释成49%的稀硫酸.求①所得稀硫酸的质量.②加入水的质量2、50g溶 2020-05-24 …
100克某硫酸溶液与13克锌巧好完全反应.求原硫酸的溶质质量分数?所得溶液中溶质质量100克某硫酸 2020-06-07 …
50gBaCI2溶液与20g4.9%稀硫酸恰好完全反应生成沉淀物多少克?BaCI2溶液中溶质的质量 2020-07-21 …
O(n1.5)与O(nlog2n)中的O是什么意思?希尔排序中提到:如果选取增量序列,则在最坏的情 2020-07-23 …
归纳:(一)在数轴上,点A表示数-3,点O表示原点,求点A、O之间的距离;根据绝对值的定义:一个数所 2020-12-07 …
从50g20%的氯化钠溶液中取出5g溶液.所取出的同业与原溶液相比,正确的是A溶液的质量为原来的1/ 2020-12-16 …
用以配制好的质量分数为6%的氯化钠溶液,配制质量分数为3%的氯化钠溶液.①计算:配制50g质量分数为 2021-01-22 …