早教吧作业答案频道 -->化学-->
某校化学兴趣小组探究SO2与FeCl3溶液的反应,所用装置如图所示(夹持仪器已略去).请回答问题:(1)该小组同学向5mLlmol/LFeCl3溶液中通人足量的SO2,溶液最终呈浅绿色,再打开分液漏斗
题目详情
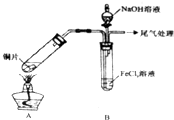
某校化学兴趣小组探究SO2与FeCl3溶液的反应,所用装置如图所示(夹持仪器已略去).请回答问题:
(1)该小组同学向5mLlmol/LFeCl3溶液中通人足量的SO2,溶液最终呈浅绿色,再打开分液漏斗活塞,逐滴加入NaOH稀溶液,则试管B中产生的实验现象是___.
(2)向5mLlmol/LFeCl3溶液中通人足量的SO2,在实验时,溶液由棕黄色变成红棕色,最终溶液呈浅绿色.
【查阅资料】Fe(HSO3)2+离子在溶液中呈红棕色,能被Fe3+氧化为SO
.
Fe(HSO3)2+与Fe3+在溶液中反应的离子方程式是___.
(3)为缩短红棕色变为浅绿色的时间,进行了如下实验:
向步骤①和步骤②所得溶液中滴加___(添化学式)试剂,溶液立即出现蓝色沉淀.
(4)综合上述实验探究过程,可以获得的实验结论:
Ⅰ.SO2与FeCl3溶液反应生成红棕色中间产物Fe(HSO3)2+离子;
Ⅱ.红棕色中间产物转变成浅绿色溶液是一个较慢的过程;
Ⅲ.___.某校化学兴趣小组探究SO2与FeCl3溶液的反应,所用装置如图所示(夹持仪器已略去).请回答问题:

(1)该小组同学向5mLlmol/LFeCl3溶液中通人足量的SO2,溶液最终呈浅绿色,再打开分液漏斗活塞,逐滴加入NaOH稀溶液,则试管B中产生的实验现象是___.
(2)向5mLlmol/LFeCl3溶液中通人足量的SO2,在实验时,溶液由棕黄色变成红棕色,最终溶液呈浅绿色.
【查阅资料】Fe(HSO3)2+离子在溶液中呈红棕色,能被Fe3+氧化为SO
.
Fe(HSO3)2+与Fe3+在溶液中反应的离子方程式是___.
(3)为缩短红棕色变为浅绿色的时间,进行了如下实验:
向步骤①和步骤②所得溶液中滴加___(添化学式)试剂,溶液立即出现蓝色沉淀.
(4)综合上述实验探究过程,可以获得的实验结论:
Ⅰ.SO2与FeCl3溶液反应生成红棕色中间产物Fe(HSO3)2+离子;
Ⅱ.红棕色中间产物转变成浅绿色溶液是一个较慢的过程;
Ⅲ.___.23

32
32
32+3+
.
Fe(HSO3)2+与Fe3+在溶液中反应的离子方程式是___.
(3)为缩短红棕色变为浅绿色的时间,进行了如下实验:
向步骤①和步骤②所得溶液中滴加___(添化学式)试剂,溶液立即出现蓝色沉淀.
(4)综合上述实验探究过程,可以获得的实验结论:
Ⅰ.SO2与FeCl3溶液反应生成红棕色中间产物Fe(HSO3)2+离子;
Ⅱ.红棕色中间产物转变成浅绿色溶液是一个较慢的过程;
Ⅲ.___.
32+3+
步骤① 往5mL1mol/LFeCl3溶液中通入SO2气体,溶液立即变为红棕色,微热在较短时间内溶液颜色变为浅绿色. 步骤② 往5mL重新配制的1mol/LFeCl3溶液(用浓盐酸酸化)中通入SO2气体,溶液立即变为红棕色,短时间内溶液颜色变为浅绿色. 步骤① 往5mL1mol/LFeCl3溶液中通入SO2气体,溶液立即变为红棕色,微热在较短时间内溶液颜色变为浅绿色. 步骤① 往5mL1mol/LFeCl3溶液中通入SO2气体,溶液立即变为红棕色,微热在较短时间内溶液颜色变为浅绿色. 32 步骤② 往5mL重新配制的1mol/LFeCl3溶液(用浓盐酸酸化)中通入SO2气体,溶液立即变为红棕色,短时间内溶液颜色变为浅绿色. 步骤② 往5mL重新配制的1mol/LFeCl3溶液(用浓盐酸酸化)中通入SO2气体,溶液立即变为红棕色,短时间内溶液颜色变为浅绿色. 32
2332+

(1)该小组同学向5mLlmol/LFeCl3溶液中通人足量的SO2,溶液最终呈浅绿色,再打开分液漏斗活塞,逐滴加入NaOH稀溶液,则试管B中产生的实验现象是___.
(2)向5mLlmol/LFeCl3溶液中通人足量的SO2,在实验时,溶液由棕黄色变成红棕色,最终溶液呈浅绿色.
【查阅资料】Fe(HSO3)2+离子在溶液中呈红棕色,能被Fe3+氧化为SO
| 2- 4 |
Fe(HSO3)2+与Fe3+在溶液中反应的离子方程式是___.
(3)为缩短红棕色变为浅绿色的时间,进行了如下实验:
向步骤①和步骤②所得溶液中滴加___(添化学式)试剂,溶液立即出现蓝色沉淀.
| 步骤① | 往5mL1mol/LFeCl3溶液中通入SO2气体,溶液立即变为红棕色,微热在较短时间内溶液颜色变为浅绿色. |
| 步骤② | 往5mL重新配制的1mol/LFeCl3溶液(用浓盐酸酸化)中通入SO2气体,溶液立即变为红棕色,短时间内溶液颜色变为浅绿色. |
Ⅰ.SO2与FeCl3溶液反应生成红棕色中间产物Fe(HSO3)2+离子;
Ⅱ.红棕色中间产物转变成浅绿色溶液是一个较慢的过程;
Ⅲ.___.某校化学兴趣小组探究SO2与FeCl3溶液的反应,所用装置如图所示(夹持仪器已略去).请回答问题:

(1)该小组同学向5mLlmol/LFeCl3溶液中通人足量的SO2,溶液最终呈浅绿色,再打开分液漏斗活塞,逐滴加入NaOH稀溶液,则试管B中产生的实验现象是___.
(2)向5mLlmol/LFeCl3溶液中通人足量的SO2,在实验时,溶液由棕黄色变成红棕色,最终溶液呈浅绿色.
【查阅资料】Fe(HSO3)2+离子在溶液中呈红棕色,能被Fe3+氧化为SO
| 2- 4 |
Fe(HSO3)2+与Fe3+在溶液中反应的离子方程式是___.
(3)为缩短红棕色变为浅绿色的时间,进行了如下实验:
向步骤①和步骤②所得溶液中滴加___(添化学式)试剂,溶液立即出现蓝色沉淀.
| 步骤① | 往5mL1mol/LFeCl3溶液中通入SO2气体,溶液立即变为红棕色,微热在较短时间内溶液颜色变为浅绿色. |
| 步骤② | 往5mL重新配制的1mol/LFeCl3溶液(用浓盐酸酸化)中通入SO2气体,溶液立即变为红棕色,短时间内溶液颜色变为浅绿色. |
Ⅰ.SO2与FeCl3溶液反应生成红棕色中间产物Fe(HSO3)2+离子;
Ⅱ.红棕色中间产物转变成浅绿色溶液是一个较慢的过程;
Ⅲ.___.23

32
32
32+3+
| 2- 4 |
Fe(HSO3)2+与Fe3+在溶液中反应的离子方程式是___.
(3)为缩短红棕色变为浅绿色的时间,进行了如下实验:
向步骤①和步骤②所得溶液中滴加___(添化学式)试剂,溶液立即出现蓝色沉淀.
| 步骤① | 往5mL1mol/LFeCl3溶液中通入SO2气体,溶液立即变为红棕色,微热在较短时间内溶液颜色变为浅绿色. |
| 步骤② | 往5mL重新配制的1mol/LFeCl3溶液(用浓盐酸酸化)中通入SO2气体,溶液立即变为红棕色,短时间内溶液颜色变为浅绿色. |
Ⅰ.SO2与FeCl3溶液反应生成红棕色中间产物Fe(HSO3)2+离子;
Ⅱ.红棕色中间产物转变成浅绿色溶液是一个较慢的过程;
Ⅲ.___.
| 2- 4 |
2-
4
2-
4
2-
4
2-
4
32+3+
| 步骤① | 往5mL1mol/LFeCl3溶液中通入SO2气体,溶液立即变为红棕色,微热在较短时间内溶液颜色变为浅绿色. |
| 步骤② | 往5mL重新配制的1mol/LFeCl3溶液(用浓盐酸酸化)中通入SO2气体,溶液立即变为红棕色,短时间内溶液颜色变为浅绿色. |
2332+
▼优质解答
答案和解析
(1)FeCl33溶液中通人足量的SO22,溶液最终呈浅绿色,溶液显酸性,再加入NaOH稀溶液,先发生中和反应,然后再反应生成氢氧化亚铁,生成二氧化硫排尽空气,氢氧化亚铁不被氧化为氢氧化铁,现象为:开始无现象,然后产生白色沉淀,
故答案为:开始无现象,然后产生白色沉淀;
(2)Fe(HSO33)2+2+被Fe3+3+氧化为SO442-2-,Fe3+3+被还原为Fe2+2+,反应离子方程式为:Fe3+3++H22O+Fe(HSO33)2+2+═2Fe2+2++SO442-2-+3H++,
故答案为:Fe3+3++H22O+Fe(HSO33)2+2+═2Fe2+2++SO442-2-+3H++;
(3)步骤①、②中Fe3+3+被还原为Fe2+2+,加入K33[Fe(CN)66]得到Fe33(Fe(CN)66)22蓝色沉淀,
故答案为:K33[Fe(CN)66];
(4)由步骤①可知,升高温度,反应速率加快,由步骤②可知提高FeCl33溶液的酸性会加快反应速率,
故答案为:升高温度、提高FeCl33溶液的酸性会加快反应速率,缩短浅绿色出现的时间.
故答案为:开始无现象,然后产生白色沉淀;
(2)Fe(HSO33)2+2+被Fe3+3+氧化为SO442-2-,Fe3+3+被还原为Fe2+2+,反应离子方程式为:Fe3+3++H22O+Fe(HSO33)2+2+═2Fe2+2++SO442-2-+3H++,
故答案为:Fe3+3++H22O+Fe(HSO33)2+2+═2Fe2+2++SO442-2-+3H++;
(3)步骤①、②中Fe3+3+被还原为Fe2+2+,加入K33[Fe(CN)66]得到Fe33(Fe(CN)66)22蓝色沉淀,
故答案为:K33[Fe(CN)66];
(4)由步骤①可知,升高温度,反应速率加快,由步骤②可知提高FeCl33溶液的酸性会加快反应速率,
故答案为:升高温度、提高FeCl33溶液的酸性会加快反应速率,缩短浅绿色出现的时间.
看了 某校化学兴趣小组探究SO2与...的网友还看了以下:
银川市鸣翠湖是国家级湿地公园,具有涵养水源、调节气候等多种功效.湿地含水丰沛,随着湿地面积的恢复增 2020-05-17 …
鸣翠湖是国家级湿地公园,具有涵养水源、调节气候等多种功效,湿地含水丰沛,随着湿地面积的恢复增大,塞 2020-05-17 …
请用所学的生物学知识回答:(1)“种豆南山下,草盛豆苗稀”这反应的是生物与生物之间的(2)白居易诗 2020-05-17 …
工业上可以用植物秸秆等富含纤维素的废弃物为原料生产葡萄糖,然后再生产乙醇,葡萄糖和乙醇都具有很多重 2020-06-20 …
“垃圾是放错地方的资源”.请应用所学习的知识参与垃圾清理与废品回收的实践活动.(1)清理垃圾时,下 2020-06-22 …
银川市鸣翠湖是国家级湿地公园,具有涵养水源、调节气候等多种功效.湿地含水丰沛,随着湿地面积的恢复增大 2020-11-13 …
高速公路上,某些司机为了降低营运成本,肆意超载,给交通安全带来极大的危害,也致使路面严重受损.请应用 2020-12-06 …
自然界中到处都存在着电解质,各种各样的电解质已经在工农业生产和社会生活中起到了愈来愈广泛的应用.请应 2020-12-18 …
高速公路上,某些司机为了降低营运成本,肆意超载,给交通安全带来极大的危害,也致使路面严重受损.请应用 2021-01-13 …
水是宝贵的自然资源,在工农业生产和日常生活中有着极其广泛的运用.请应用所学知识回答下列问题:(1)有 2021-01-21 …