早教吧作业答案频道 -->化学-->
碳和碳的化合物在生产、生活中有重要作用,甲醇水蒸气重整制氢系统可能发生下列三个反应:①CH3OH(g)⇌CO(g)+2H2(g)△H1=+90.8kJ/mol②CH3OH(g)+H2O(g)⇌CO2(g)+3H2(g)△H2=+49kJ/mol③C
题目详情
碳和碳的化合物在生产、生活中有重要作用,甲醇水蒸气重整制氢系统可能发生下列三个反应:
①CH3OH(g)⇌CO(g)+2H2(g)△H1=+90.8kJ/mol
②CH3OH(g)+H2O(g)⇌CO2(g)+3H2(g)△H2=+49kJ/mol
③CO(g)+H2O(g)⇌CO2(g)+H2(g)△H3
回答下列问题:
(1)△H3=___;
(2)以CO、H2为原料合成甲醇的反应为:CO(g)+2H2(g)═CH3OH(g).在体积均为2L的三个恒容密闭容器Ⅰ、Ⅱ、Ⅲ中,分别都充入1molCO和2molH2,三个容器的反应温度分别为T1、T2、T3且恒定不变.图1为三个容器中的反应均进行到5min时H2的体积分数示意图,其中有一个容器反应一定达到平衡状态.CO的平衡转化率在不同压强下随温度的变化如图2所示.
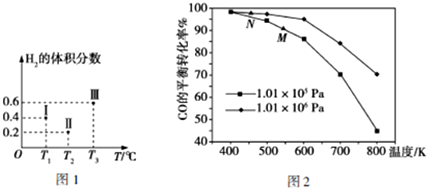
①0~5min时间内容器II中用CH3OH表示的反应速率为___.
②三个容器中一定达到平衡状态的是容器___.
③平衡常数最大的是容器___.
④工业实际合成CH3OH生产中,常用图中M点而不是N点对应的反应条件,运用化学反应速率和平衡知识,同时考虑生产实际,说明选择该反应条件的理由:___.
(3)甲醇使用不当会造成其对水质的污染,用电化学可消除这种污染,其原理是电解CoSO4、稀硫酸和CH3OH混合溶液,将Co2+氧化成Co3+,Co3+再将CH3OH氧化成CO2.
①电解时,阳极的电极反应式为___;
②Co3+氧化CH3OH的离子方程式为___.
(4)控制反应条件,反应①中的产物也可以用来合成甲醇和二甲醚,其中合成二甲醚的化学方程式为3H2(g)+3CO(g)═CH3OCH3(g)+CO2(g),对于气相反应,用某组分(B)的平衡分压(PB)代替物质的量浓度(cB)也可以表示平衡常数(记作KP),水煤气合成二甲醚的反应的平衡常数表达式为KP=___.
①CH3OH(g)⇌CO(g)+2H2(g)△H1=+90.8kJ/mol
②CH3OH(g)+H2O(g)⇌CO2(g)+3H2(g)△H2=+49kJ/mol
③CO(g)+H2O(g)⇌CO2(g)+H2(g)△H3
回答下列问题:
(1)△H3=___;
(2)以CO、H2为原料合成甲醇的反应为:CO(g)+2H2(g)═CH3OH(g).在体积均为2L的三个恒容密闭容器Ⅰ、Ⅱ、Ⅲ中,分别都充入1molCO和2molH2,三个容器的反应温度分别为T1、T2、T3且恒定不变.图1为三个容器中的反应均进行到5min时H2的体积分数示意图,其中有一个容器反应一定达到平衡状态.CO的平衡转化率在不同压强下随温度的变化如图2所示.

①0~5min时间内容器II中用CH3OH表示的反应速率为___.
②三个容器中一定达到平衡状态的是容器___.
③平衡常数最大的是容器___.
④工业实际合成CH3OH生产中,常用图中M点而不是N点对应的反应条件,运用化学反应速率和平衡知识,同时考虑生产实际,说明选择该反应条件的理由:___.
(3)甲醇使用不当会造成其对水质的污染,用电化学可消除这种污染,其原理是电解CoSO4、稀硫酸和CH3OH混合溶液,将Co2+氧化成Co3+,Co3+再将CH3OH氧化成CO2.
①电解时,阳极的电极反应式为___;
②Co3+氧化CH3OH的离子方程式为___.
(4)控制反应条件,反应①中的产物也可以用来合成甲醇和二甲醚,其中合成二甲醚的化学方程式为3H2(g)+3CO(g)═CH3OCH3(g)+CO2(g),对于气相反应,用某组分(B)的平衡分压(PB)代替物质的量浓度(cB)也可以表示平衡常数(记作KP),水煤气合成二甲醚的反应的平衡常数表达式为KP=___.
▼优质解答
答案和解析
(1)①CH3OH(g)⇌CO(g)+2H2(g)△H2=+90.8kJ/mol
②CH3OH(g)+H2O(g)⇌CO2(g)+3H2(g)△H2=+49kJ/mol
依据盖斯定律计算②-①得到③:CO(g)+H2O(g)⇌CO2(g)+H2(g)△H3=-41.8 kJ/mol,
故答案为:-41.8 kJ/mol;
(2)①设反应生成的甲醇物质的量为x,
CO(g)+2H2(g)═CH3OH(g)
开始(mol):1 2 0
转化(mol):x 2x x
平衡(mol):1-x 2-2x x
到5min时,氢气的体积分数为0.2,则
=0.2,则x=
,
则v=
=
=0.0875mol/(L•min),
故答案为:0.0875mol/(L•min);
②达到平衡状态时氢气的转化率最大,氢气的体积分数最小,II对应的氢气的体积分数最小,所以II可能达到了平衡状态;
故答案为:II;
故答案为:0.0875mol/(L•min);②Ⅲ;(1分)
③由图2可知,升高温度CO的转化率减小,即向逆反应移动,所以该反应为放热反应,温度越低,反应向正方向进行的程度越大,K越大,已知I的温度最低,则其K最大;
故答案为:I;
④相对于N点而言,采用M点,温度在500-600K之间,温度较高,反应速率较快,氢气的平衡转化率也较高,压强为常压对设备要求不高,
故答案为:相对于N点而言,采用M点,温度在500-600K之间,温度较高,反应速率较快,氢气的平衡转化率也较高,压强为常压对设备要求不高;
(3)①其原理是电解CoSO4、稀硫酸和CH3OH的混合溶液,将Co2+氧化为Co3+,Co3+再将CH3OH氧化成CO2.
电解池中该电极上发生失电子的氧化反应,电极反应为:Co2+-e-═Co3+,
故答案为:Co2+-e-═Co3+;
②Co3+将甲醇氧化为二氧化碳,本身被还原为Co,即6Co3++CH3OH+H2O═CO2↑+6Co2++6H+;
故答案为:6Co3++CH3OH+H2O═CO2↑+6Co2++6 H+;
(4)3H2(g)+3CO(g)⇌CH3OCH3(g)+CO2(g),反应的平衡常数KP表达式为生成物平衡分压幂次方乘积除以反应物平衡分压幂次方乘积
;
故答案为:
.
②CH3OH(g)+H2O(g)⇌CO2(g)+3H2(g)△H2=+49kJ/mol
依据盖斯定律计算②-①得到③:CO(g)+H2O(g)⇌CO2(g)+H2(g)△H3=-41.8 kJ/mol,
故答案为:-41.8 kJ/mol;
(2)①设反应生成的甲醇物质的量为x,
CO(g)+2H2(g)═CH3OH(g)
开始(mol):1 2 0
转化(mol):x 2x x
平衡(mol):1-x 2-2x x
到5min时,氢气的体积分数为0.2,则
| 2-2x |
| (1-x)+(2-2x)+x |
| 7 |
| 8 |
则v=
| △c |
| △t |
| ||||
| 5min |
故答案为:0.0875mol/(L•min);
②达到平衡状态时氢气的转化率最大,氢气的体积分数最小,II对应的氢气的体积分数最小,所以II可能达到了平衡状态;
故答案为:II;
故答案为:0.0875mol/(L•min);②Ⅲ;(1分)
③由图2可知,升高温度CO的转化率减小,即向逆反应移动,所以该反应为放热反应,温度越低,反应向正方向进行的程度越大,K越大,已知I的温度最低,则其K最大;
故答案为:I;
④相对于N点而言,采用M点,温度在500-600K之间,温度较高,反应速率较快,氢气的平衡转化率也较高,压强为常压对设备要求不高,
故答案为:相对于N点而言,采用M点,温度在500-600K之间,温度较高,反应速率较快,氢气的平衡转化率也较高,压强为常压对设备要求不高;
(3)①其原理是电解CoSO4、稀硫酸和CH3OH的混合溶液,将Co2+氧化为Co3+,Co3+再将CH3OH氧化成CO2.
电解池中该电极上发生失电子的氧化反应,电极反应为:Co2+-e-═Co3+,
故答案为:Co2+-e-═Co3+;
②Co3+将甲醇氧化为二氧化碳,本身被还原为Co,即6Co3++CH3OH+H2O═CO2↑+6Co2++6H+;
故答案为:6Co3++CH3OH+H2O═CO2↑+6Co2++6 H+;
(4)3H2(g)+3CO(g)⇌CH3OCH3(g)+CO2(g),反应的平衡常数KP表达式为生成物平衡分压幂次方乘积除以反应物平衡分压幂次方乘积
| p(CH3OCH3)p(CO2) |
| p3(H2)p3(CO) |
故答案为:
| p(CH3OCH3)p(CO2) |
| p3(H2)p3(CO) |
看了碳和碳的化合物在生产、生活中有...的网友还看了以下:
1.氢氧化钙与非金属氧化物生成什么?2.氢氧化钙与酸反应?3.氢氧化钠与盐反应?4.氢氧化钙与盐反 2020-05-02 …
有40克氢气和氧气的混合气体,在密闭容器内点火后生成了36克水,求混合气体中氢气和氧气的质量可能是 2020-05-13 …
常见化学方程式书写:1.氢气在氯气中燃烧生成氯化氢2.氧化汞分解3.氢氧化钠与硫酸铜溶液反应4.氢 2020-06-04 …
分子式为C7H10的开经烃A,可发生下列反应:(1)A经催化加氢可生成3一乙基戊烷.(2)A与硝酸 2020-06-11 …
在699K时,反应氢气和碘蒸汽反应生成碘化氢的平衡常数Kp等于55.3,如果将2.00mol氢气和 2020-06-12 …
请问原子分光光度法(氢化物法)中的载液在哪一步用到?(拒绝复制粘贴)3.砷的测定(氢化物法)测定条 2020-07-05 …
求一下化学方程式的写法.1.有黑色氧化物生成的氧化反应的化学方程式2.生成两种单质的分解反应的化学 2020-07-12 …
是这样的.上课的时候老师说铝离子和氢氧根可以发生两种反应,分别是铝离子和氢氧根离子比例是1:3时生成 2020-11-03 …
一般烃分子脱去两个氢原子形成烯键是吸热反应,脱氢形成双键约需112kJ/mol~125kJ/mol的 2020-11-05 …
有下列反应.1:铁和硫酸铜生成铜和硫酸铁.2:氧化钙和水生成氢氧化钙.3:氢氧化钡和硫酸生成硫酸和水 2021-02-09 …