早教吧作业答案频道 -->化学-->
(1)将锌片和铜片浸入稀硫酸中组成原电池,两电极间连接一个电流计.观察到的现象为:,铜片上的电极反应式为:.若该电池中两电极的总质量为60g,工作一段时间后,电路中转移
题目详情
(1)将锌片和铜片浸入稀硫酸中组成原电池,两电极间连接一个电流计.观察到的现象为:___,
铜片上的电极反应式为:___.若该电池中两电极的总质量为60g,工作一段时间后,电路中转移了0.4mol电子,则产生氢气的体积(标准状况)为___L,两电极的总质量为___g.
(2)铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等.
①写出FeCl3溶液腐蚀印刷电路铜板的离子方程式___.
②若将①中的反应设计成原电池,请画出原电池的装置图,标出正、负极,并写出电极反应式.
负极反应___,正极反应___.
铜片上的电极反应式为:___.若该电池中两电极的总质量为60g,工作一段时间后,电路中转移了0.4mol电子,则产生氢气的体积(标准状况)为___L,两电极的总质量为___g.
(2)铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等.
①写出FeCl3溶液腐蚀印刷电路铜板的离子方程式___.
②若将①中的反应设计成原电池,请画出原电池的装置图,标出正、负极,并写出电极反应式.
负极反应___,正极反应___.
▼优质解答
答案和解析
(1)将锌片和铜片浸入稀硫酸中组成原电池,锌为负极失电子发生氧化反应,反应失为:Zn-2e-=Zn2+;铜为正极氢离子得电子发生还原反应,反应失为:2H++2e-=H2↑,所以观察到的现象为锌片溶解,铜片上有气泡产生,电流计发生偏转;电路中转移了0.4mol电子,则产生氢气的体积(标准状况)为
×22.4=4.48L,溶解的锌为
×65=13g,则两电极的总质量为60-13=47g,
故答案为:锌片溶解,铜片上有气泡产生,电流计发生偏转;2H++2e-=H2↑;4.48;47;
(2)①Fe3+有强氧化性,能把金属铜氧化成铜离子,自身被还原成 Fe2+,反应方程式为2Fe3++Cu=2Fe2++Cu2+,故答案为:2Fe3++Cu=2Fe2++Cu2+;
②设计成原电池时,负极上发生氧化反应,正极上发生还原反应,该电池反应中三价铁离子得电子发生还原反应,所以正极上的电极反应式为Fe3++e-=Fe2+(或2Fe3++2e-=2Fe2+),铜失电子发生氧化反应,所以负极上的电极反应式为Cu=2Cu2++2e-(或Cu-2e-=Cu2+);
电池反应中发生氧化反应的金属作负极,所以铜作负极,不如负极活泼的金属或导电的非金属作正极,可选石墨作正极,发生还原反应的电解质溶液作原电池的电解质溶液,所以该原电池图为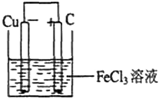 ,故答案为:
,故答案为: ;Cu-2e-=Cu2+;Fe3++e-=Fe2+;
;Cu-2e-=Cu2+;Fe3++e-=Fe2+;
| 0.4 |
| 2 |
| 0.4 |
| 2 |
故答案为:锌片溶解,铜片上有气泡产生,电流计发生偏转;2H++2e-=H2↑;4.48;47;
(2)①Fe3+有强氧化性,能把金属铜氧化成铜离子,自身被还原成 Fe2+,反应方程式为2Fe3++Cu=2Fe2++Cu2+,故答案为:2Fe3++Cu=2Fe2++Cu2+;
②设计成原电池时,负极上发生氧化反应,正极上发生还原反应,该电池反应中三价铁离子得电子发生还原反应,所以正极上的电极反应式为Fe3++e-=Fe2+(或2Fe3++2e-=2Fe2+),铜失电子发生氧化反应,所以负极上的电极反应式为Cu=2Cu2++2e-(或Cu-2e-=Cu2+);
电池反应中发生氧化反应的金属作负极,所以铜作负极,不如负极活泼的金属或导电的非金属作正极,可选石墨作正极,发生还原反应的电解质溶液作原电池的电解质溶液,所以该原电池图为
 ,故答案为:
,故答案为: ;Cu-2e-=Cu2+;Fe3++e-=Fe2+;
;Cu-2e-=Cu2+;Fe3++e-=Fe2+;
看了(1)将锌片和铜片浸入稀硫酸中...的网友还看了以下:
工业上制备纯净的氯化锌时,将含杂质的氯化锌溶于过量的盐酸中,为了除去杂质需要调节溶液的pH到4,应 2020-05-13 …
(1)把FeCl3溶液蒸干灼烧最后的产物是。(2)工业上制备纯净的氯化锌时,将含杂质的氯化锌溶于过 2020-05-13 …
工业上制备纯净的氯化锌时,需将含杂质的氯化锌溶于过量的盐酸中,为了除去杂质需调节溶液的pH为4,应 2020-05-13 …
工业上制备纯净的氯化锌时,将含杂质的氯化锌溶于过量的盐酸中,为了除去杂质需要调节溶液的pH到4,应 2020-05-13 …
工业上制备纯净的氯化锌时,将含杂质的氯化锌溶于过量盐酸中,为了除去杂质需调节溶液的pH到4,应加入 2020-05-13 …
ALCL3能存在与酸中吗为什么? 2020-05-14 …
带锈的螺帽,如何将上面的铁锈除去?能否将其长时间放入稀盐酸中,为什么?写出反应的方程式.. 2020-06-26 …
工业盐酸中常混有少量的FeCl3而呈黄色.为测定某工业盐酸中FeCl3的含量进行如下实验:取该工业 2020-07-16 …
浓硫酸和双氧水会反映么?浓硫酸中S为高价,容易得到电子,而双氧水中有一个O容易失去电子,两者混一起会 2020-11-10 …
硫酸是工业生产中最为重要的产品之一,在化学工业的很多领域都要用到浓硫酸.(1)在硫酸工业生产中,我国 2020-11-24 …