早教吧作业答案频道 -->化学-->
金属钼(Mo)是人体及动植物必需的微量元素,也可以增强合金的某些机械性能和耐腐蚀性,图1是模拟化工生产中制备金属钼的实验流程图(已知钼酸为难溶于水和酸的黄色晶体):请回答
题目详情
金属钼(Mo)是人体及动植物必需的微量元素,也可以增强合金的某些机械性能和耐腐蚀性,图1是模拟化工生产中制备金属钼的实验流程图(已知钼酸为难溶于水和酸的黄色晶体):
请回答下列问题:
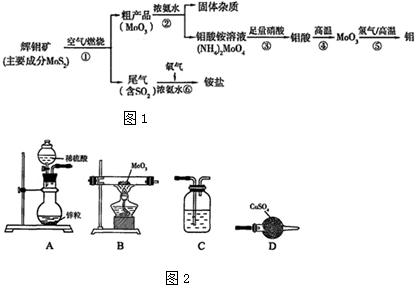
(1)步骤②和③反应完成后都要进行的操作是___;步骤④用于盛放钼酸的仪器名称为___.
(2)在灼烧辉钼矿时发生化学反应:2MoS2+7O2
2MoO3+4SO2,当有1mol MoS2反应时,还原剂失去电子的物质的量为___;步骤②中发生反应的离子方程式___.
(3)若实验需要480mL 2mol/L的稀硝酸,则配制时需要用量筒取___mL63%的浓硝酸(密度ρ=1.4g/cm3),所有仪器除量筒外还有烧杯、玻璃棒、胶头滴管和___.
(4)步骤⑥吸收尾气生成铵盐的化学方程式为___,检验该铵盐中阴离子所需要的试剂为___.
(5)若选用如图2装置完成步骤⑤的反应,同时检验该反应的氧化产物.
①实验步骤如下:连接好仪器,检查装置气密性,装入药品,打开分液漏斗活塞___→___→___→___(请按正确的先后顺序填入下列步骤的代号).
a.收集气体并检验其纯度 b.停止加热,充分冷却
c.加热反应一段时间 d.关闭分液漏斗活塞,停止通氢气
②装置C中所盛的试剂是___(填试剂名称);证明装置B中已经发生反应的现象是___.
请回答下列问题:

(1)步骤②和③反应完成后都要进行的操作是___;步骤④用于盛放钼酸的仪器名称为___.
(2)在灼烧辉钼矿时发生化学反应:2MoS2+7O2
| ||
(3)若实验需要480mL 2mol/L的稀硝酸,则配制时需要用量筒取___mL63%的浓硝酸(密度ρ=1.4g/cm3),所有仪器除量筒外还有烧杯、玻璃棒、胶头滴管和___.
(4)步骤⑥吸收尾气生成铵盐的化学方程式为___,检验该铵盐中阴离子所需要的试剂为___.
(5)若选用如图2装置完成步骤⑤的反应,同时检验该反应的氧化产物.
①实验步骤如下:连接好仪器,检查装置气密性,装入药品,打开分液漏斗活塞___→___→___→___(请按正确的先后顺序填入下列步骤的代号).
a.收集气体并检验其纯度 b.停止加热,充分冷却
c.加热反应一段时间 d.关闭分液漏斗活塞,停止通氢气
②装置C中所盛的试剂是___(填试剂名称);证明装置B中已经发生反应的现象是___.
▼优质解答
答案和解析
辉钼矿(主要成分是MoS2)在空气中燃烧生成MoO3和SO2,尾气含SO2用浓氨水吸收,并通入氧气生成硫酸铵;MoO3加浓氨水生成钼酸铵溶液,过滤除去杂质,在钼酸铵溶液中加足量硝酸,生成钼酸,钼酸为难溶于水和酸的黄色晶体,过滤得到钼酸晶体高温分解生成MoO3,在高温条件下用氢气还原得到金属钼;
(1)步骤②和③反应完成后都要进行的操作是分离固体和液体混合物,所以操作名称为过滤;步骤④是高温分解钼酸,则所用的仪器为坩埚;
故答案为:过滤;坩埚;
(2)2MoS2+7O2
2MoO3+4SO2,当有1mol MoS2反应时,消耗的氧气的物质的量问3.5mol,则转移电子的物质的量为3.5mol×4=14mol;MoO3与浓氨水反应生成钼酸铵,其反应的离子方程式为:2NH3•H2O+MoO3═2NH4++MoO42-+H2O;
故答案为:14mol;2NH3•H2O+MoO3═2NH4++MoO42-+H2O;
(3)质量分数为65%、密度为1.4g/cm3的浓硝酸的浓度为:c=
mol/L=14.4mol/L,若实验需要480mL 2mol/L的稀硝酸,需要用500ml容量瓶配制,则2mol/L的稀硝酸的体积为500ml,溶液稀释前后溶质的物质的量不变,则:C浓•V浓=C稀•V稀,14.4mol/L×V浓=2mol/L×0.5L
解得:V浓=0.0714L=71.4ml;
故答案为:71.4;500ml容量瓶;
(4)SO2用浓氨水吸收,并通入氧气生成硫酸铵,其反应的化学方程式为:4NH3•H2O+2SO2+O2═2(NH4)2SO4+2H2O;检验硫酸根离子应该先用稀盐酸排除干扰离子,再加氯化钡溶液,若有白色沉淀,则说明有硫酸根离子;
故答案为:4NH3•H2O+2SO2+O2═2(NH4)2SO4+2H2O;稀盐酸和氯化钡溶液;
(5)用锌与稀硫酸反应生成氢气,再浓硫酸干燥,然后再加热条件下还原MoO3,最后用无水硫酸铜检验生成的水;
①实验步骤如下:连接好仪器,检查装置气密性,装入药品,打开分液漏斗活塞,收集氢气并检验其纯度,然后加热B装作反应一段时间,停止加热,继续通氢气,充分冷却,然后关闭分液漏斗活塞,停止通氢气,则操作顺序为a→c→b→d;
故答案为:a、c、b、d;
②装置C中所盛的试剂是用于干燥氢气,则试剂为浓硫酸;氢气还原MoO3生成水蒸气,使无水硫酸铜变蓝色;
故答案为:浓硫酸;无水硫酸铜变蓝色.
(1)步骤②和③反应完成后都要进行的操作是分离固体和液体混合物,所以操作名称为过滤;步骤④是高温分解钼酸,则所用的仪器为坩埚;
故答案为:过滤;坩埚;
(2)2MoS2+7O2
| ||
故答案为:14mol;2NH3•H2O+MoO3═2NH4++MoO42-+H2O;
(3)质量分数为65%、密度为1.4g/cm3的浓硝酸的浓度为:c=
| 1000×1.4×65% |
| 63 |
解得:V浓=0.0714L=71.4ml;
故答案为:71.4;500ml容量瓶;
(4)SO2用浓氨水吸收,并通入氧气生成硫酸铵,其反应的化学方程式为:4NH3•H2O+2SO2+O2═2(NH4)2SO4+2H2O;检验硫酸根离子应该先用稀盐酸排除干扰离子,再加氯化钡溶液,若有白色沉淀,则说明有硫酸根离子;
故答案为:4NH3•H2O+2SO2+O2═2(NH4)2SO4+2H2O;稀盐酸和氯化钡溶液;
(5)用锌与稀硫酸反应生成氢气,再浓硫酸干燥,然后再加热条件下还原MoO3,最后用无水硫酸铜检验生成的水;
①实验步骤如下:连接好仪器,检查装置气密性,装入药品,打开分液漏斗活塞,收集氢气并检验其纯度,然后加热B装作反应一段时间,停止加热,继续通氢气,充分冷却,然后关闭分液漏斗活塞,停止通氢气,则操作顺序为a→c→b→d;
故答案为:a、c、b、d;
②装置C中所盛的试剂是用于干燥氢气,则试剂为浓硫酸;氢气还原MoO3生成水蒸气,使无水硫酸铜变蓝色;
故答案为:浓硫酸;无水硫酸铜变蓝色.
看了金属钼(Mo)是人体及动植物必...的网友还看了以下:
如图的漫画《反腐“组合拳”》启示我们()A.对腐败行为要加重处罚B.惩治腐败必须多管齐下C.反腐只 2020-07-12 …
糠酸又称呋喃甲酸,在食品工业作防腐剂,还可用于合成树脂或医药、香料等的中间体.以米槺或玉米芯提取的 2020-07-24 …
集合(用描述法表示集合)被5除余1的正整数集合答:{X|X=5n+1,X属于N}(答案上后面写的是 2020-07-29 …
关于合金的说法正确的是()A.合金是一种纯净物B.合金中只含有金属元素C.合金的强度、硬度一般比组成 2020-11-20 …
2014年11月23日央视曝光毒腐竹事件后,某市为保证本地生产的腐竹合格,制定和实施了“放心豆制品” 2020-11-21 …
下列说法不正确的是()A.天然气作为化工原料主要用于合成氨和生产甲醇B.甲醛的水溶液俗称福尔马林,具 2020-11-23 …
回答关于合成氨工业生产方面的问题:在合成塔中安置热交换器的目的是:①预热原料气以利于NH3的合成;② 2020-12-06 …
关于合金的说法正确的是()A.合金中只含有金属元素B.铁锈是一种合金C.合金的强度、硬度、熔点一般比 2020-12-19 …
生活中处处有化学.下列说法正确的是()A.pH<6.5的是酸雨,能腐蚀大理石等建筑物B.图书档案着火 2021-01-01 …
千页豆腐的做法大全千叶豆腐适合老人吃吗 2021-04-05 …